Biomimetic Actuation and Tissue Growth
Biologische Materialien können ihre Form und Struktur im Laufe ihres Lebens verändern. Bekannte Beispiele dazu sind die Entwicklung von Organen während der Embryogenese, die Heilung von verletztem Gewebe aber auch passive, durch Feuchtigkeitsänderung angetriebene Pflanzenbewegung wie der Öffnungsmechanismus eines Kiefernzapfens. Diese Veränderungen basieren auf der Bildung von neuem Gewebe und/oder auf heterogener Verformung von bereits bestehendem Gewebe. Die sich daraus ergebende makroskopische Formänderung ist geometrieabhängig – von der Geometrie der unmittelbaren Umgebung und von der Geometrie, die beschreibt wie die sich verformenden Gewebe innerhalb des Materials selbst angeordnet sind. Diesem allgemeinen Thema nähert sich die Gruppe mit zwei Ansätzen:
- Materialaufbau von natürlichen und biomimetischen Aktuatoren
- Einfluss der Geometrie auf kollektives Zellverhalten und/oder Gewebewachstum

Biomimetische Aktuatorik
Ausgangspunkt unserer Arbeit sind Pflanzensysteme, die durch (passive) Adsorption von Wasser hervorgerufene, komplexe Bewegungsmuster zeigen, wie beispielsweise das Öffnen und Schließen der Schuppen eines Kiefernzapfens oder die Bewegung der Grannen des Weizens (siehe auch die Forschungsgruppe von Michaela Eder ). Die Pflanzenorgane dieser Systeme sind Struktur und Motor in einem. Die Bewegung selbst wird durch die geometrische Anordnung von Geweben, die unterschiedliches Quellverhalten zeigen, gesteuert. Wir sind in erster Linie daran interessiert, mechanische Modelle für einfache biomimetische Systeme zu entwickeln und diese Modelle auf die natürlichen Pflanzensysteme anzuwenden. Weiters wollen wir den Gestaltungsraum (desgin-space) für Antriebe, die auf der Materialarchitektur basieren, erforschen. Die aufgedeckten Bauprinzipien sollen für die Entwicklung neuer biomimetischer Verbundwerkstoffe genutzt werden.
Referenzen:
- Harrington, M. J., et al. (2011). Origami-like unfolding of hydro-actuated ice plant seed capsules. Nature Communications, 2, 337–7.
- Stoychev, G., et al. (2012). Shape-Programmed Folding of Stimuli-Responsive Polymer Bilayers. ACS Nano, 6, 3925-2934.
- Stoychev, G., et al. (2013) Hierarchical multi-step folding of polymer bilayers, Advanced Functional Materials, 23, 2295-2300
- Guiducci, L., et al. (2014) Pressurized honeycomb as soft-actuators: a theoretical study, Journal of the Royal Society Interface, 11: 20140458.
- Razghandi, K., et al. (2014) Hydro-actuation of ice plant seed capsules powered by water uptake, Bioinspired, Biomimetic and Nanobiomaterials 3, 169-182.
- Zhao, Q., et al. (2014) An instant multi-responsive porous polymer actuator operating via solvent molecule sorption, Nature Communications, 5, 4293.
- Zhao, Q., et al. (2015) Porous poly(ionic liquid) actuator with ultra-high sensitivity to solvents, Advanced Materials 27, 2913-2917.
- Guiducci, L., et al. (2015) The Geometric Design and Fabrication of Actuating Cellular Structures, Advanced Materials Interfaces, 2, 1500011.
- Stoychev, G., et al. (2016) Hole-programmed superfast multistep actuation of polymer bilayers, Advanced Functional Materials, , 26, 7733-7739.
- Gong, J., et al. (2017) Hierarchically arranged helical fiber actuators derived from commercial cloth, Advanced Materials DOI: 10.1002/adma.201605103
Gewebewachstum
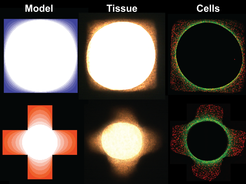
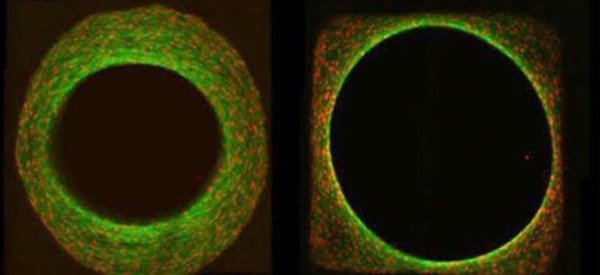
Gewebewachstum wird durch biochemische Faktoren gesteuert, aber auch physikalische Eigenschaften der lokalen Zellumgebung, wie z. B. Steifigkeit und Form haben wesentlichen Einfluss darauf. Wir gehen der Frage nach, ob die unmittelbare Geometrie der Zellumgebung, im Speziellen die Krümmung der Oberfläche des Substrates, die Proliferationsrate und das daraus resultierende Gewebewachstum kontrolliert. Unser Ziel dabei ist es, theoretische Modelle, die Gewebewachstum beschreiben mit in-vitro Zellkulturexperimenten zu kombinieren um die beobachtete Abhängigkeit des Gewebewachstums von der Krümmung zu verstehen. Die Modelle sollen zu einem tieferen Verständnis des Einflusses der Geometrie auf Prozesse wie Knochenheilung oder Knochenumbau beitragen (siehe auch die Forschungsgruppen von Wolfgang Wagermaier und Richard Weinkamer).
Referenzen:
- Rumpler, M., et al. (2008). The effect of geometry on three-dimensional tissue growth. Journal of The Royal Society, Interface, 5(27), 1173–1180.
- Dunlop, J. W. C., et al. (2010). A theoretical model for tissue growth in confined geometries. Journal of the Mechanics and Physics of Solids, 58(8), 1073–1087.
- Bidan C. M. et al. (2012). How Linear Tension Converts to Curvature: Geometric Control of Bone Tissue Growth . PLoS ONE 7(5), e36336, doi:10.1371/journal.pone.0036336
- Bidan C.M. et al. (2013). Geometry as a factor for tissue growth: Towards shape optimization of tissue engineering scaffolds. Advanced HealthCare Materials 2, 186-194.
- Gamsjaeger, E., et al. (2013) The role of surface stress on the kinetics of tissue growth in confined geometries. Acta Biomaterialia 9, 5531-5543.
- Bidan, C, M., et al, (2013) A three dimensional model for tissue deposition on complex surfaces, Computer Methods in Biomechanics and Biomedical Engineering, 16, 1056-1070.
- Fischer, F. D., et al. (2015) Tissue growth controlled by geometric boundary conditions: a simple model recapitulating aspects of callus formation and bone healing, Journal of the Royal Society Interface, 12, 20150108.
- Herklotz, M., et al, (2015), Availability of extracellular matrix biopolymers determines space-filling growth of human mesenchymal stem cells in vitro, Biomaterials, 60, 121-129.
- Bidan, C. M., et al, (2016), Gradual conversion of cellular stress patterns into pre-stressed matrix architecture during in vitro tissue growth. Journal of the Royal Society Interface, 2016. 13: 20160136
- Werner, M., et al, (2017), Surface Curvature Differentially Regulates Stem Cell Migration and Differentiation via Altered Attachment Morphology and Nuclear Deformation, Advanced Science, 2017, 4, 1600347.
- Ehrig, S., et al (2017), Curvature controlled defect dynamics in active systems, accepted in Physical Review E

