Automatisierte chemische Synthese von Kohlenhydraten
Forschungsbericht (importiert) 2009 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Einleitung
Kohlenhydrate und deren biologische Funktionen sind im Vergleich zu anderen wichtigen Biomolekülen erstaunlich wenig erforscht. Ein Grund dafür ist die besondere Schwierigkeit, die mit der Herstellung oder Gewinnung komplexer Kohlenhydratmoleküle in der nötigen Reinheit und Menge verbunden ist. In den letzten zehn Jahren sind enorme Fortschritte in der chemischen Synthese von Kohlenhydraten erzielt worden. Diese Entwicklung hat es ermöglicht biochemische Fragestellungen, insbesondere in Bezug auf komplexe Kohlenhydrate, massiv voranzutreiben. In der Abteilung für Biomolekulare Systeme werden neben allgemeiner Entwicklung neuer Strategien zur chemischen Herstellung von Kohlenhydraten auch Akzente auf die Anwendung synthetischer Zuckermoleküle im biologischen Bereich gesetzt. Schwerpunkte wie die Entwicklung Kohlenhydrat-basierter Impfstoffe oder der Einsatz chemisch hergestellter Oligosaccharide als Werkzeuge für die Glykobiologie und Glykoimmunologie sind ebenfalls Forschungsschwerpunkte der Abteilung.
Automatisierte Kohlenhydratsynthese

Aufgrund ihrer chemischen Beschaffenheit, die zahlreiche reaktive Hydroxylgruppen aufweist, stellen komplexe Kohlenhydratmoleküle eine besondere Herausforderung für den synthetischen Chemiker dar. Mit der Entwicklung des weltweit ersten Oligosaccharid-Syntheseautomaten [1] hat die Abteilung für Biomolekulare Systeme nicht nur ein essentielles Problem in der organischen Synthese gelöst, sondern vor allem eine leistungsfähige Plattform kreiert, die die Kohlenhydratforschung an der Grenzfläche zwischen Chemie, Biologie und Medizin deutlich vereinfacht (Abb. 1). Mit diesem Instrument wird die Synthese komplexer Oligosaccharide in Tagen statt, wie in der Vergangenheit, in Jahren ermöglicht [2]. Die Weiterentwicklung des Geräts wird momentan in allen Aspekten mit großen Fortschritten vorangetrieben, um das Produktspektrum auf noch komplexere Glykokonjugate wie Glykoproteine, Glykolipide und Heparin zu erweitern. Das Ziel, das Gerät als kommerzielle Maschine zu entwickeln, die einen definierten Satz an Zuckerbausteinen verwendet um die meisten Oligosacchariden zusammenzusetzen, kann somit in naher Zukunft erreicht werden. Dies würde biologischen und medizinischen Forschungsgruppen die Möglichkeit bieten mit dem Gerät ganz ohne Hilfe von Kohlenhydratchemikern selbst komplexe Moleküle zu synthetisieren.
Synthetische Oligosaccharide als Werkzeug für die Glykobiologie
Die Tatsache, dass komplexe Oligosaccharide in einer großen Vielfalt und geeigneten Menge durch chemische Synthese zur Verfügung gestellt werden können, hat den Weg für die Anwendung neuer analytischer Methoden eröffnet. Methoden wie Microarrays, die bislang exklusiv für Forschungsbereiche wie Genomics und Proteomics angewendet wurden, können so auch in der Glykobiologie routinemäßig eingesetzt werden. Synthetische Oligosaccharide können auch an Trägermaterial gekoppelt werden, um spezifische Bindungspartner aus biologischen Extrakten durch Affinitätschromatographie zu isolieren und zu charakterisieren. Zusätzlich ermöglichen Farbstoff-markierte synthetische Oligosaccharide in vitro und in vivo Studien mittels mikroskopischer Analysen oder tomographischer Methoden. Die Abteilung für Biomolekulare Systeme hat in diesem Zusammenhang durch den Einsatz von Glykoarrays Pionierarbeiten in den folgenden Bereichen geleistet.
1- Identifizierung spezifischer HIV-Oligosaccharide für eine Zucker-basierte Impfstoffentwicklung gegen die AIDS-Erkrankung
2- Charakterisierung von Bindungspartnern bei Zucker-Lektin-Interaktionen
3- Untersuchung der Spezifität sowie der Resistenzproblematik von Aminoglykosidenantibiotika
4- Screening von Blutproben nach Krankheitsmarkern
5- Detektion pathogener Bakterien im Blut und anderen Körperflüssigkeiten.
Synthetische Kohlenhydrate als Impfstoffkandidaten gegen Infektionskrankheiten
Ein entscheidender Einsatzbereich von synthetischen Oligosacchariden ist die Verwendung der chemisch hergestellten Zuckermoleküle als Impfstoffkandidaten. Die Oberfläche aller lebenden Zellen inklusiv aller pathogenen Mikroorganismen enthält eine große Anzahl an Glykanen und Glykokonjugaten. Diese spielen meist bei Infektionsprozessen durch Interaktion mit entsprechenden Bindungspartnern auf der Wirtszellmembran eine tragende Rolle und stellen damit wichtige Angriffspunkte für die Entwicklung neuwertiger Impfstoffe und Medikamente dar. Bei der Malaria-Erkrankung beispielsweise ist es ein Zuckermolekül, das sogenannte Glykosylphosphatidyl Inositol (GPI), das für die Erscheinung der tödlichen zerebralen Malaria verantwortlich ist. Dieses Molekül wurde chemisch hergestellt und als antitoxischer Impfstoffkandidat erfolgreich in einem Mausmodell der schweren Malaria eingesetzt. Es wurde deutlich gezeigt, dass spezifisch gegen den Zucker generierte Antikörper die geimpften Mäuse von dem Eintreten der tödlichen zerebralen Malaria bewahren konnten [3]. Weiterhin konnte mittels synthetischer GPI-Glykan-Arrays gezeigt werden, dass eine Infektion mit dem Malaria-Erreger beim Menschen zur Produktion von spezifisch gegen das GPI-Glykan gerichteten Antikörpern führt (Abb. 2) [4]. Diese Ergebnisse lieferten einen wichtigen Rückhalt zur Kohlenhydrat-basierten Impfstoffhypothese bei der Malaria-Erkrankung. Die Synthese des Impfstoffs ist mittlerweile in Zusammenarbeit mit einer Biotech-Firma in großen Mengen gelungen, und die ersten klinischen Versuche am Menschen sind für 2011 geplant. Neben dem Malaria-Impfstoffprojekt werden Kohlenhydrat-basierte Impfstoffe gegen weitere Infektionskrankheiten wie Anthrax, Leishmaniose, Tuberkulose, Vogelgrippe und zahlreiche bakterielle Erkrankungen entwickelt.
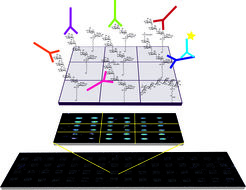
Biochemie der Lektin-Glykan-Interaktion bei Infektionskrankheiten
Neben der Entwicklung von Kohlenhydrat-basierten Impfstoffen um Infektionskrankheiten zu bekämpfen besteht auch die Möglichkeit, die Interaktion zwischen Zuckermolekülen und entsprechenden bindenden Proteinen während des Infektionsprozesses mit spezifischen Inhibitoren zu blockieren. Um solche Inhibitoren effektiv zu entwerfen und zu entwickeln, muss der molekulare Mechanismus der Interaktion zwischen den Partnern gründlich untersucht werden. Wir versuchen in diesem Rahmen durch Untersuchung der Struktur-Funktions-Zusammenhänge von Lektinen ihre Bindungseigenschaften zu charakterisieren. Mittels der Phage-Display-Technologie werden kurze Peptide isoliert, die mit der gleichen Spezifität wie das Zuckermolekül an das Lektin binden. Nach Strukturanalyse werden diese Peptide chemisch zu besseren Inhibitoren optimiert.
Glykoimmunologie
Neben den oben erwähnten Möglichkeiten können synthetische Zucker zur gezielten Wirkstoffapplikation und zum Targeting von C-Typ-Lektinrezeptoren (CLRs) auf Antigen-präsentierenden Zellen genutzt werden.
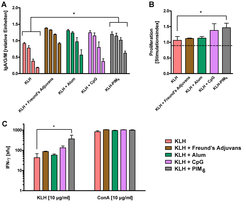
So wurde mittels der Glykoarray-Technologie gezeigt, dass synthetische Zuckerstrukturen aus Mycobacterium tuberculosis, die Phosphatidylinositolmannoside (PIMs), an CLRs wie DC-SIGN binden (5). Die Immunisierung von Mäusen mit dem Modellantigen KLH unter Verwendung von PIM6 als Wirkstoffverstärker (Adjuvans) zeigte, dass PIM6 die Immunantwort gegen das Modellantigen signifikant stimulierte, indem es zu verstärkter Antigenaufnahme, T-Zellaktivierung und Antikörperproduktion führte (Abb. 3). Diese Ergebnisse verdeutlichen, dass CLRs auf Antigen-präsentierenden Zellen gezielt durch synthetische Liganden aktiviert werden können.
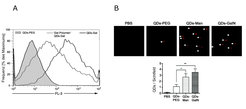
Ein weiteres Beispiel für das gezielte Einbringen von Substanzen in Zellen durch das Ausnutzen der Bindung von Zucker-Liganden an CLRs ist die Verwendung von Zucker-gekoppelten Quantum Dots (QDs). Dabei wurden QDs verwendet, die mit terminalen D-Galactose-Monosacchariden funktionalisiert waren, um den Asialoglykoprotein-Rezeptor in Leberzellen zu binden. Auch in vivo war ein spezifisches Targeting der Leber durch die Verwendung von D-Gal/D-GalN-funktionalisierten QDs möglich (Abb. 4).
Sequenzdefinerte Glykomimetika
Neben der Synthese von natürlichen Zuckern gewinnen auch das Design und die Synthese sogenannter Mimetika zunehmend an Bedeutung im Bereich der Glycomics. Die zwei wichtigsten Klassen der Zuckermimetika sind die Glykodendrimere und die linearen Neoglykopolymere. Die Glykodendrimere bestehen aus einzelnen Zucker-Bausteinen oder kleineren Oligosacchariden, die an ein dendritisches Grundgerüst angeknüpft sind. Neoglykopolymere bestehen aus einer Polymerkette, die meist in der Seitenkette Zuckereinheiten trägt.
Im Gegensatz zu den natürlichen Zuckern sind vor allem die linearen Neoglykopolymere einfacher und in größerer Menge synthetisch zugänglich und können durch gezielte Optimierung sogar deren biologische Wirkung deutlich übertreffen. Hierbei spielt vor allem die multivalente Präsentation und die lokale Vororganisation eine wichtige Rolle. Klassische Polymersynthese liefert jedoch nur stark polydisperse Neoglykopolymere und die Kontrolle über Funktionalität und Struktur ist unzureichend.
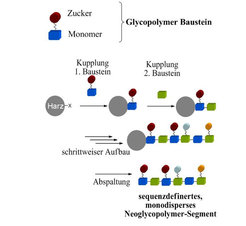
Im Rahmen der Emmy Noether-Nachwuchsgruppe wird daher mithilfe der Festphasensynthese ein neuer Ansatz zur Darstellung monodisperser, multifunktionaler Neoglykopolymere realisiert. Der kontrollierte schrittweise Aufbau aus speziell dargestellten Monomer-Bausteinen erlaubt hier das gezielte Positionieren verschiedener Funktionalitäten und den Aufbau einer Monomersequenz im Neoglykopolymer-Segment (Abb. 5). Dies ermöglicht sowohl den Aufbau von hoch-definierten linearen Neoglykopolymeren als auch von komplexeren Überstrukturen wie Dendrimeren, Blockcopolymeren oder Hydrogelen. Mithilfe solcher hoch-definierten Systeme können nun systematisch Struktur-Funktionsbeziehungen im biologischen System untersucht und diese Information zur Entwicklung neuartiger Wirkstoffe und Wirkstofftransportsysteme z.B. für die Krebstherapie verwendet werden.
Zusammenfassung und Ausblick
Der von der Abteilung für Biomolekulare Systeme des Max-Planck-Instituts für Kolloid- und Grenzflächenforschung entwickelte Zuckersynthesizer hat neue Maßstäbe im Bereich der Kohlenhydratchemie gesetzt. Die so hergestellten komplexen Oligosaccharide haben bereits einen breiten Anwendungsbereich gefunden wie etwa bei der Entwicklung von Zucker-basierten Impfstoffen oder bei Glykoarrays zur Untersuchung spezifischer Interaktionen zwischen Oligosacchariden und entsprechenden bindenden Proteinen. Es ist anzunehmen, dass die hiermit gegebene Möglichkeit, genau definierte Zuckermoleküle in nötigen Mengen und Reinheit zu generieren, die Zuckerforschung in gleichem Maße prägen wird wie einst die Einführung von Peptid- und DNA-Synthesizer die Peptid- und Nukleinsäurenforschung. Obwohl die meisten Anwendungen der synthetisierten komplexen Oligosaccharide vor allem im biologischen bzw. medizinischen Bereich stattfinden, hat die Ausbreitung in andere Bereiche wie in die Polymerforschung oder die Nanotechnologie schon begonnen.


![Immunisierung von Mäusen mit dem Modellantigen KLH, gekoppelt an PIM6. C57BL/6-Mäuse wurden subkutan mit KLH in Gegenwart der genannten Adjuvantien oder PIM6 immunisiert. A, Am Tag 17 nach der Immunisierung wurde die Menge an Anti-KLH-Antikörpern in seriellen Verdünnungen der Sera bestimmt. B, Die T-Zellproliferation nach Restimulation mit dem Modellantigen KLH wurde gemessen. C, Am Tag 20 nach der Immunisierung wurde die Zahl an IFN-γ produzierenden Zellen mittels ELISpot gemessen [5]. Immunisierung von Mäusen mit dem Modellantigen KLH, gekoppelt an PIM6. C57BL/6-Mäuse wurden subkutan mit KLH in Gegenwart der genannten Adjuvantien od](https://www.mpg.de/322654/original-1293750039.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MzIyNjU0fQ%3D%3D--13a494115aca99181561e9fad6583dee041c2731)
![Spezifisches Targeting von Leberzellen mit D-Gal/D-GalN-funktionalisierten Quantum Dots (QDs). A, HepG2-Zellen wurden mit Kontroll-QDs (QDs-PEG) oder Gal-QDs inkubiert. Die Rezeptor-vermittelte Aufnahme der Gal-QDs in die HepG2-Zellen wurde durch Vorinkubation mit einem PLL-Gal-Polymer blockiert. B, Spezifisches Leber-Targeting mit D-Mannose (D-Man) und D-Galactosamin (D-GalN) QDs in vivo [6]. Spezifisches Targeting von Leberzellen mit D-Gal/D-GalN-funktionalisierten Quantum Dots (QDs). A, HepG2-Zellen wurden mit Kontroll-QDs (QDs-PEG) oder](https://www.mpg.de/322710/original-1293749663.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MzIyNzEwfQ%3D%3D--2a0f6332da35bde1e6e51c8b1f0932a41337016c)
![Schematische Darstellung der Festphasensynthese sequenzdefinierter, monodisperser Polymere und Neoglykopolymere [7]. Schematische Darstellung der Festphasensynthese sequenzdefinierter, monodisperser Polymere und Neoglykopolymere [7].](https://www.mpg.de/322766/original-1293750080.jpg?t=eyJ3aWR0aCI6MzQxLCJmaWxlX2V4dGVuc2lvbiI6ImpwZyIsIm9ial9pZCI6MzIyNzY2fQ%3D%3D--b36006beec175eefbf4d7166905e0d2d10632e9e)